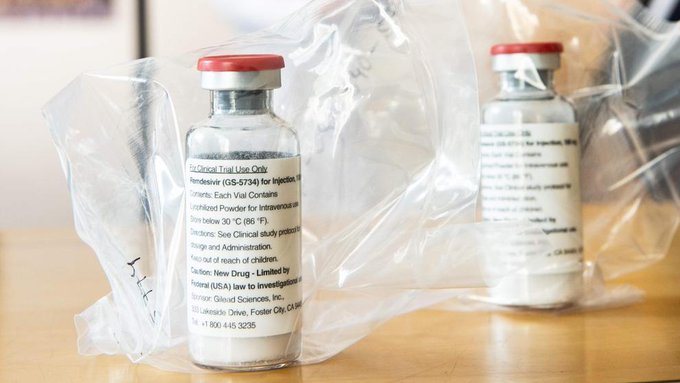
El presidente Donald Trump anunció este viernes que la Administración de Drogas y Alimentos de Estados Unidos (FDA) había otorgado una autorización a Gilead Sciences Inc para el uso de emergencia de su medicamento antiviral experimental Remdesivir para tratar pacientes con Covid-19.
Durante una reunión con el presidente ejecutivo de Gilead, Daniel O’Day, el republicano calificó la medida como un primer paso importante y dijo que la compañía estaba donando 1 millón de frascos del medicamento para ayudar a los pacientes.
“Estoy contento de anunciar que Gilead obtuvo de la FDA la autorización urgente para el uso del remdesivir”, indicó Trump en La Casa Blanca.
El Remdesivir, según un estudio, facilita una recuperación más rápida de los pacientes con Covid-19, por lo que su autorización permitirá a los hospitales estadounidenses recetarlo para los enfermos más graves, por ejemplo.
El fármaco fue aprobado tras un estudio en que los pacientes infectados por Covid-19 se recuperaban más rápido, algo que fue anunciado por el director del Instituto Nacional de Alergias y Enfermedades Infecciosas de Estados Unidos, Anthony Fauci.
Sin embargo, la FDA aclaró que “no hay ningún producto disponible aprobado por la FDA para tratarel Covid-19” en términos generales, y que el uso del Remdesivir puede beneficiar a algunos pacientes hospitalizados.
Esta noticia, anunciada por el propio Donald Trump, se enmarcó en la amenaza de imponer nuevos aranceles punitivos a Pekín, acusado por Washington de haber permitido, a través de su mala gestión de la crisis, que el virus se propagara.