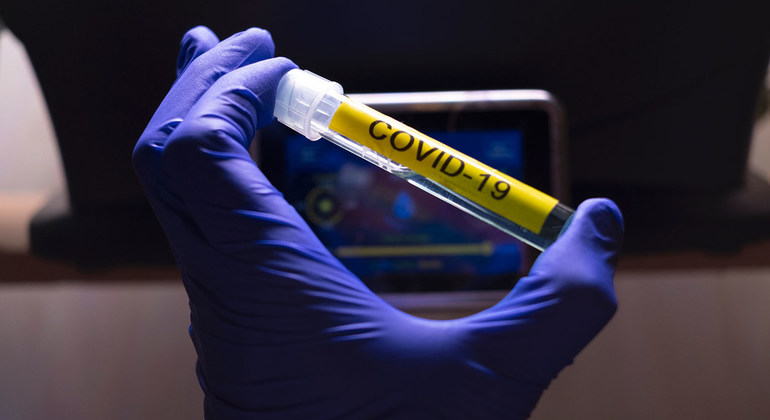
Nueve importantes desarrolladores de vacunas de Estados Unidos y Europa se comprometieron este martes a mantener los estándares científicos con los que se llevarán a cabo sus inmunizaciones experimentales, en medio de una carrera mundial apresurada para contener la pandemia.
We are committed to developing a #COVID19 #vaccine that is both safe & effective, but success goes beyond that. Our teams will continue to work urgently, but we will never compromise our high standards in the pursuit of a vaccine: https://t.co/FPhTdVgsPe #WeStandWithScience pic.twitter.com/mOYkWyO80c
— Pfizer Inc. (@pfizer) September 8, 2020
Las compañías, incluidas Pfizer, GlaxoSmithKline y AstraZeneca, en una declaración conjunta hicieron un “compromiso histórico… para mantener la integridad del proceso científico mientras trabajan por posibles presentaciones regulatorias globales y aprobaciones de las primeras vacunas contra el COVID-19”.
El movimiento inusual de prometer seguir reglas establecidas subraya un debate altamente politizado sobre qué acción se necesita para frenar rápidamente la propagación de la enfermedad mortal y reactivar los negocios y comercios globales.
El jefe de la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) dijo el mes pasado que el proceso normal de aprobación de una vacuna contra el COVID-19 podría pasarse por alto, siempre que los funcionarios estuvieran convencidos de que los beneficios superan los riesgos, lo que provocó un llamado a la precaución por parte de la Organización Mundial de la Salud (OMS).
#JNJ is proud to share our commitment to upholding the integrity of the scientific process in the development of a #COVID19 vaccine. Rigorous science and safety must be the priority in vaccine development. #WeStandWithScience, and encourage @AstraZeneca to stand with us. https://t.co/3NnE2QmYh0 pic.twitter.com/XtosCUH5DR
— Johnson & Johnson (@JNJNews) September 8, 2020
Los desarrolladores a nivel mundial aún tienen que producir datos de pruebas a gran escala que muestren las infecciones reales en los participantes, sin embargo, Rusia aprobó una vacuna contra el COVID-19 el mes pasado, lo que llevó a algunos expertos occidentales a criticar la falta de pruebas.
“Al firmar el compromiso, Johnson & Johnson, AstraZeneca, BioNTech, GlaxoSmithKline, Merck, Moderna, Inc., Novavax, Inc., Pfizer Inc. y Sanofi subrayan un compromiso conjunto para desarrollar y probar posibles vacunas para COVID-19 de acuerdo con altos estándares éticos y principios científicos sólidos con respecto a la realización de nuestros ensayos clínicos y el rigor de nuestros procesos de fabricación”, se lee en la declaración conjunta.
Las empresas añaden que se comprometen a enviar sus vacunas para su aprobación o autorización de uso de emergencia solo después de demostrar su seguridad y eficacia a través de un estudio clínico de Fase 3 diseñado y realizado para cumplir con los requisitos de autoridades reguladoras expertas.
El director de la china Sinovac Biotech dijo que la mayoría de sus trabajadores y sus familias ya han probado una vacuna experimental desarrollada por la firma, en el marco del programa de uso de emergencia del país.
“Queremos que se sepa que también en la situación actual no estamos dispuestos a comprometer la seguridad y la eficacia”, dijo uno de los firmantes, Ugur Sahin, director ejecutivo del socio alemán de Pfizer, BioNTech.
Our Chief Medical Officer, GSK Vaccines, Thomas Breuer explains why we’ve joined other biopharm companies in pledging to uphold the integrity of the scientific process in the research and development of a #COVID19 vaccine. https://t.co/7Y0jDQ1Qac #WeStandWithScience pic.twitter.com/bcqnfuF3QJ
— GSK (@GSK) September 8, 2020
BioNTech y Pfizer han planteado la posibilidad de revelar datos fundamentales de los ensayos en octubre, lo que podría colocarlos en el centro de la compleja política presidencial de Estados Unidos, previo a las elecciones del 3 de noviembre.
Según el comunicado, las nueve empresas se comprometen a seguir las pautas establecidas de las autoridades expertas reguladoras, como la FDA.
Los reguladores han enfatizado que no tomarían atajos, sino que priorizarían la carga de trabajo de revisión y permitirían pasos de desarrollo en paralelo que normalmente se manejarían consecutivamente